氨基糖苷類抗生素為廣效性抗生素,是臨床上治療細菌性感染的重要藥物,其作用機制是與細菌核醣體結合抑制蛋白質的生成,進而殺死或阻止細菌持續滋長。抗生素上的「氨基」是與核醣體結合辨識的重要化學官能基,研究數據顯示,若病原菌對此類抗生素已產生抗藥性,往往可在此菌中發現有能將氨基乙醯化的抗藥性基因。
達爾文曾說:「最終能生存下來的物種,不是最強的、也不是最聰明的,而是最能適應改變的物種」,有一部分細菌在演化競爭中發展出氨基糖苷類抗生素來攻擊競爭對手,對手便運用氨基乙醯化作用化解攻勢,競爭者再演化出新型態的氨基,如:亞氨甲醯化或亞氨二乙醯化等修飾機制加以反擊,可說無懼於乙醯化的失活並維持與核醣體相當程度的親和力。
本院基因體研究中心李宗璘教授與福井縣立大學濱野吉十教授合作形成一個國際研究團隊共同探討鏈絲菌素衍生物生合成路徑,本研究經由體內基因剃除及體外酵素反應實驗,找到並證實了亞氨甲醯化或亞氨二乙醯化酶(Orf1)的生化功能,並能將選取的數種氨基糖苷類抗生素亞氨甲醯化或亞氨二乙醯化產生新穎的產物(圖一)。
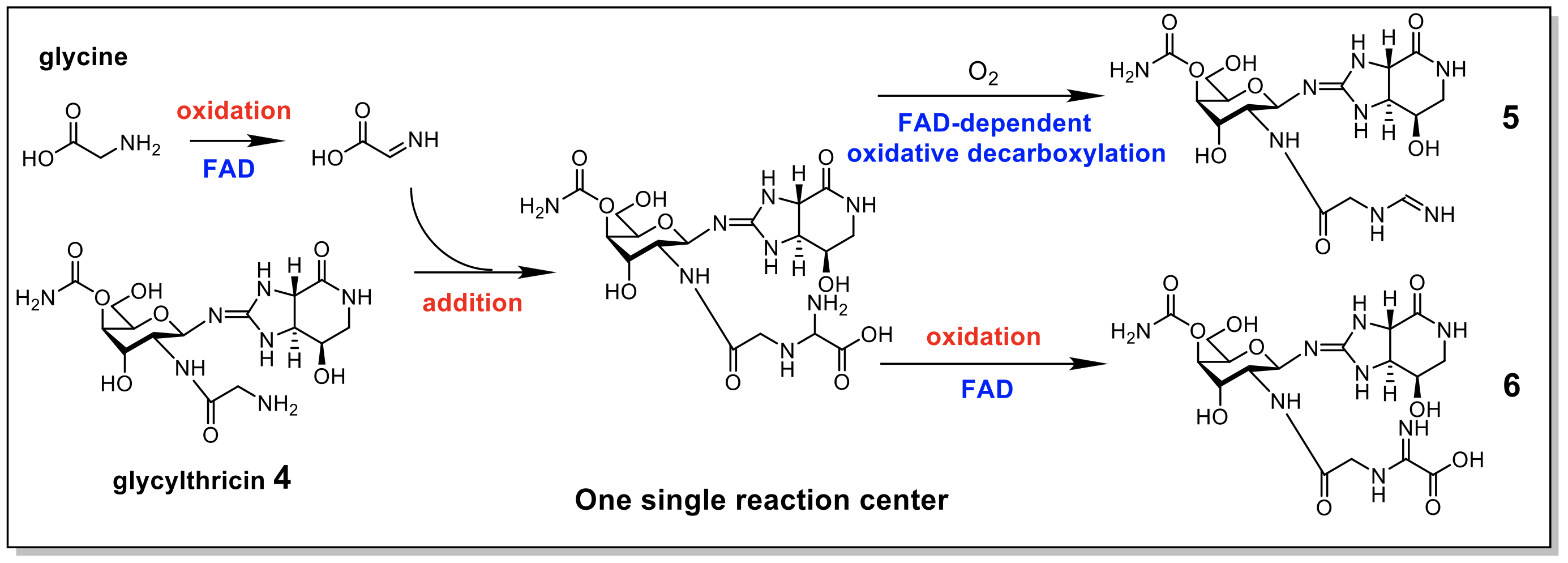 |
| 圖一、先前預測Orf1催化藉由多步驟反應由甘氨酸與抗生素(4)形成亞氨甲醯化(5)或亞氨二乙醯化(6)。 |
為了瞭解該酵素的作用機制,研究人員解析複合晶體結構,發現甘氨酸與鏈絲菌素前驅物的結合區相距甚遠,不利加成反應的進行,且加成後的中間產物無法經由FAD進行傳統的脫羧及二次氧化反應(圖二-A)。出人意表地,該團隊發現氧化甘氨酸經與酵素半胱氨酸的硫原子形成首見的受質與酵素間的”氮氧硫”共價鍵架橋(圖二-B),不同於近來被報導的蛋白質”氮氧硫” 架橋,其是一種經由活性氧物質與蛋白質中的離氨酸及半胱氨酸間自發形成的可逆性轉譯後修飾,通常與蛋白功能的調控有關。
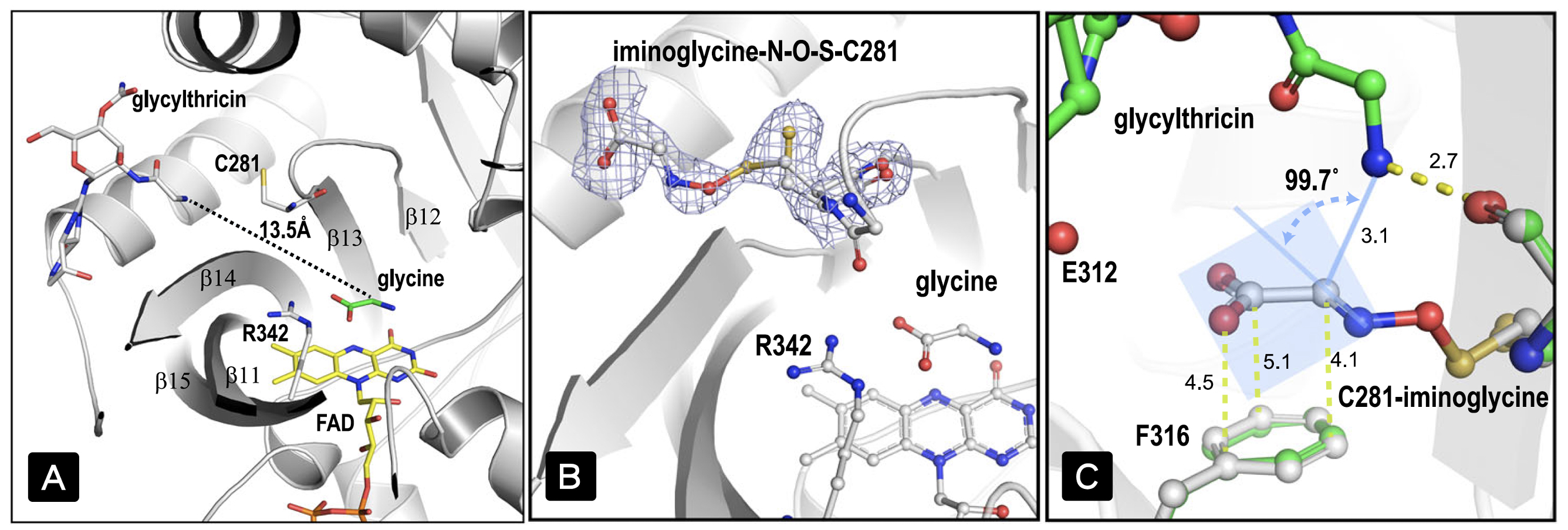 |
| 圖二、兩受質結合區、半胱氨酸與氧化甘氨酸之氮氧硫橋與重疊結構顯示之加成反應區域。 |
此次所發現的氮氧硫架橋,係甘氨酸經由FAD氧化後形成的活性物質,透過酵素分子內專一孔道傳送到鏈絲菌素前驅物結合區,與氧化的半胱氨酸次磺酸基形成氮氧硫橋,重疊抗生素受質與氮氧硫橋晶體結構發現,氮與碳原子間有合適的距離與角度(圖二-C),利於加成反應發生形成產物,成為氮氧硫橋直接參與酵素催化反應的第一個發現案例。
研究團隊更透過點突變分析,發現靠近氮氧硫橋的兩個氨基酸殘基扮演重要的反應調控角色,突變株的主要產物會由亞氨甲醯化變成亞氨二乙醯化抗生素,推測此兩氨基酸能夠促進脫羧協同的脫去反應,使鍵斷裂發生在氮氧之間;使用不同的鏈絲菌素在氧18同位素水中反應,得知蛋白質共價鍵斷裂在氧硫之間可再生氧18次磺酸基,另一方面產物經脫水後即形成亞氨二乙醯化,因而控制鍵結斷裂的位置(氮氧與氧硫之間)可使酵素產生兩種不同產物(圖三),與傳統FAD酵素經由氧化性脫羧的機制截然不同。
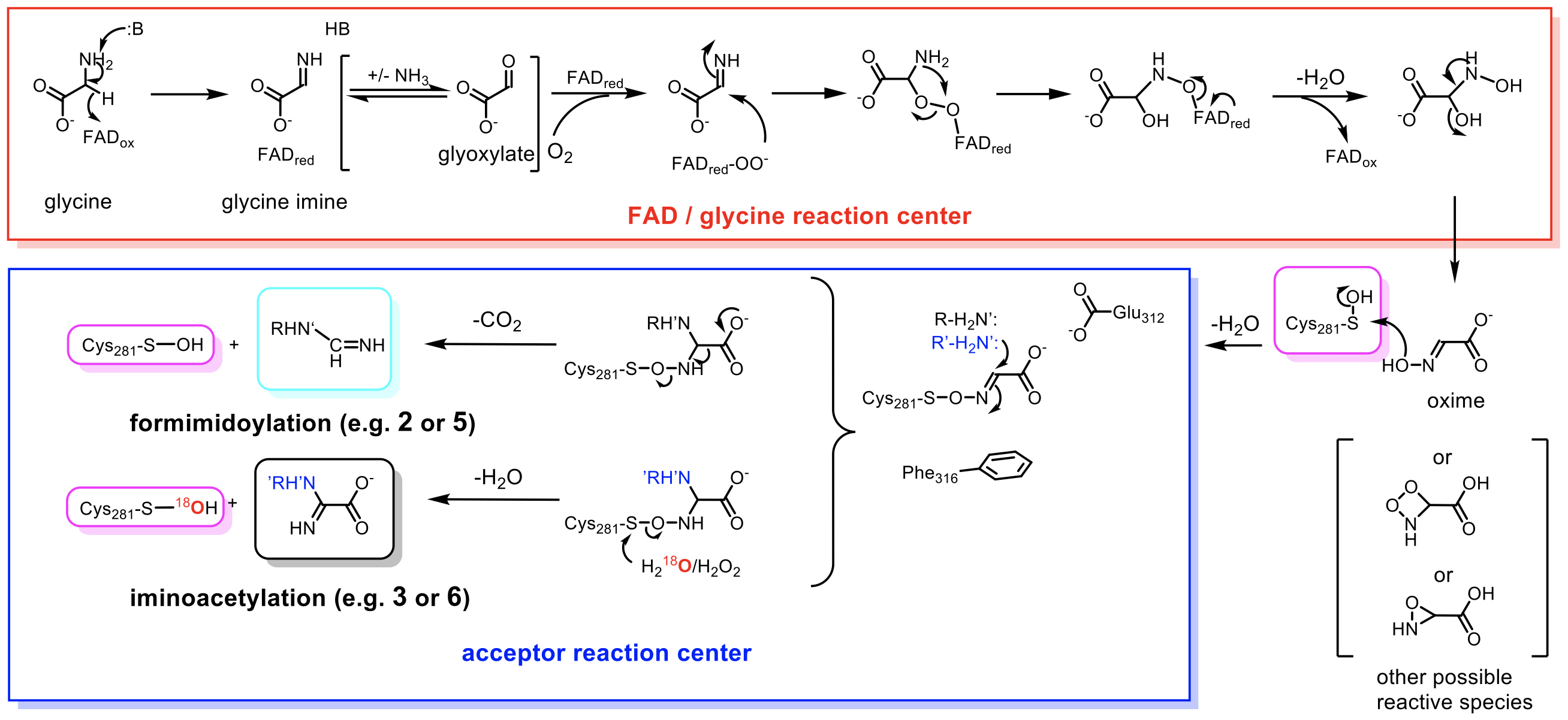 |
| 圖三、依實驗結果推測之Orf1反應機制。 |
最終研究團隊證實此類修飾機制能夠避免抗生素被抗性基因轉乙醯化而失去治療功效,為未來新一代氨基糖苷類抗生素的研發,提供一種新型態的修飾選擇。
本研究成果是由基因體中心李宗璘教授、張七鳳博士、福井縣立大學濱野吉十教授、日本北海道大學大利徹教授與陽明交通大學張晉源教授所組的跨校國際團隊協力共同完成,並發表在國際知名期刊Nature Communications,第一作者為王詠霖博士。
論文全文“N-Formimidoylation/-iminoacetylation modification in aminoglycosides requires FAD-dependent and ligand-protein NOS bridge dual chemistry”可於線上閱讀:https://www.nature.com/articles/s41467-023-38218-w