走進基因體中心五樓,張子文老師的實驗室,一個不大不小的空間,研究生和助理加起來不到十個人,經常同進同出,讓人覺得挺友善的。空氣中,似乎感覺不出什麼壓力。這會是那個報載與生技公司簽訂高額Anti-CεmX專利授權金,令人稱羨的團隊?
由於與生技公司簽約之事,廣為媒體所報導,張老師大方回應中心網頁製作小組的要求,與團隊同仁針對這個成果,作一個多面向的經驗分享。
張子文老師已是產學有成的知名科學家,他所發明的抗過敏藥物Xolair註一,已在世界許多國家核准用于重度哮喘。該藥在台灣命名為『樂無喘』,在2008年納入健保給付,造福許多長期嚴重氣喘患者。這個基因工程製劑,也是衛生署核發新藥上市許可證以來,第一個由國人所研發的藥品。這個藥物所針對的標的,是由人體B淋巴細胞所產生的E型免疫球蛋白IgE。
簡而言之,在原始的環境下,IgE是人體免疫系統為了防禦寄生蟲而產生的,不幸的是,在現代工業化的過程中,人的居住環境與生活形態作劇烈改變,衛生也變好了,有些人的免疫系統因而對無害的環境物質產生IgE,引致發炎、氣管收縮等反應,造成各種過敏疾病。因此,血液中對某些環境物質具結合特異性的IgE濃度,是醫學上評估過敏體質及過敏疾病的重要指標。
以往,科學家以為IgE是過敏反應的結果,直到張老師首先針對IgE發明了具特殊結合特異性的單株抗體,繼而鍥而不捨的研究證明了只要能抑制體內的IgE,就能解除過敏的現象。
Xolair 就是Anti-IgE的抗體藥物,它的主要作用就在於中和與抑制血液及體液中的IgE。
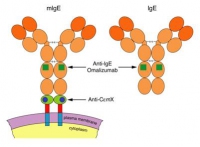
IgE有兩種,一種為膜鑲嵌型IgE,一顆B細胞大約有200000至500000個膜鑲嵌型IgE;另一種,就是已分佈在全身各處的分泌型IgE,也就是大部份在人體內會造成過敏反應的IgE。當Xolair進入人體後,絕大部分的抗體藥物分子,會與散佈游離於全身的IgE產生作用。
雖然Xolair已被證實具有治療功效,但是,總有斬草不除根,春風吹又生以及在某些病人體內IgE量遠高於可用藥量的問題。要解決這個問題的根本之道,就要直搗細胞繼續產生IgE的源頭。
IgE於1967年被兩個免疫學家研究群發現;20年之後,在1987年,張子文老師發明Anti-IgE的治療方策;繼而於1991年,他發現了膜鑲嵌型IgE上有一含有52個氨基酸的從所未知的片段,將之命名為CεmX。CεmX實為"ConstantεMembrane X"的縮寫,也就是"每個人都有、插在細胞膜上的ε型過敏分子的未明區塊"的意思。對於專注於免疫學研究的張老師而言,CεmX是控制IgE生產的一個“漂亮的標的物”。
2006年,張子文老師加入基因體研究中心,當時他在清華大學的研究生,也跟著他到中心的實驗室繼續學習。此次的專利,就是張老師與三個學生共同申請與享有的。
這其中,陳君柏在大學期間,就對免疫學有特別的興趣,大二時就已修完張老師開給大四學生的免疫課程。去年,他已順利的取得博士學位,目前仍然在張老師的實驗室內,作Anti-CεmX後續發展工作。
吳哲豪,仍然是一個博士生,大學時學的是化學與材料工程,有別於同班同學,他放棄收入相對優渥的工程師就業市場,選擇了一條較艱難但是符合他的興趣的路。
洪福信,大學時讀的是化學,也是根據自己的興趣,在研究所時進入生命科學領域,先從暑期自修再經選課補修了分子生物與免疫學,才得以進入張老師的免疫研究實驗室。
在這Anti-CεmX的研究工作內,他們三人各有各的專門興趣,他們共同的心願是找尋能兼具學術以及實用價值的題目,作為研究的目標;互相分享心得、腦力激蕩的過程,也是他們共同依循的方法。對他們而言,忠實於自己的興趣,得到充份自由的發想空間,與一個互相討論分享的環境,是他們從各有想法到分工合作的關鍵。
此研究的起源在於陳君柏發現原始第一代的Anti-CεmX抗體無法結合表現膜嵌型IgE的B細胞,因而興起研發第二代Anti-CεmX抗體的念頭。然而,既然想要有所突破,必須用新的方法來產生新的單株抗體 (monoclonal antibody)。
此時,洪福信正致力於表現與純化膜嵌型IgE,欲用於解析CεmX的結構。他認為膜嵌型IgE上的CεmX具有近似天然的構型,因此,使用此蛋白作為抗原,用以免疫小鼠,是能成功製備Anti-CεmX抗體的重要突破。
小鼠產生抗體之後,利用Hybridoma技術,篩選了近4000株不同的抗體,陳君柏透過許多的功能分析,包括分析抗體是否可以標的表現膜嵌型IgE的B細胞、經由細胞凋亡(Apoptosis)毒殺表現膜嵌型IgE的B細胞、引致細胞抑殺作用(ADCC)、以及抑制B細胞產生IgE等,一關又一關的驗證,進而發現只有在標的CεmX上特定位置的第二代Anti-CεmX抗體,才會具備上述的功能。這一系列篩檢過程及抗體功能分析,已於2010年發表於Journal of Immunology 期刊(2010 Vol.184:1748-1756, "Unique Epitopes on CεmX in IgE–B Cell Receptors Are Potentially Applicable for Targeting IgE-Committed B Cells” )。
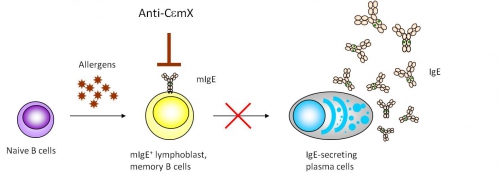
圖3說明了Anti-CεmX的作用機制。未受過抗原刺激的B細胞(naïve B cells)受到過敏原的刺激,會先分化成表現膜嵌型IgE的細胞,進一步再分化成專司生產分泌型IgE的漿細胞(plasma cells),Anti-CεmX抗體可抑殺表現膜嵌型IgE的B細胞,導致此分化途徑受阻進而降低IgE的生成。
最後,他們選擇了一株最具潛力的Anti-CεmX抗體,命名為“4B12”,決定往下進行抗體人源化的步驟,朝臨床試驗前進。
吳哲豪負責抗體人源化(humanization)的工作,將這個4B12抗體內大部分來自於小鼠的氨基酸序列,替換成人類IgG1抗體的氨基酸序列,以避免將來使用4B12抗體藥物的病人對小鼠蛋白產生抗體反應,以致消耗抗體藥物。這人源化過程必須確保這改造過的4B12抗體仍保有原本抗體與對結合CεmX所具的專一性及親和力。
張老師表示,他不會硬性指定他的學生作題目,他的教學方式著重啟發學生,讓他們各自找尋研究的題目,然後自動自發的形成研究團隊,從事研究工作。因此,在這Anti-CεmX的專利陳君柏等三位學生都是具有足夠貢獻的發明人。
如報載,Anti-CεmX抗過敏抗體新藥專利已授權給國內生技公司進行接下來的新藥開發工作。眼看一個在實驗室所凝聚的力量,逐步推動著這個發明,走上造福病人的道路。對於所有學習從事研究生涯的學生和後博士研究員,這確實是一個很具激勵性的典範。
未來,如果一切開發新藥的工作順利完成,如願達到通過新藥上市的門檻,不但參與貢獻的學生和老師可以獲得里程碑款項,亦可以替中研院帶來藥物銷售的權利金。
參與這計畫的同仁們都表示,新藥開發的過程才開始,這路途很長,在藥物還未被核准上市之前一直是個未知數;以Xolair來說,從研究到臨床、上市,一共花了十六年。目前,他們能夠確定的,就是將保持專注的研究態度,繼續全心投入研究工作。
即便如此,張子文老師的團隊,在『台灣生技起飛鑽石行動方案』裡,已經寫下值得許多老師和學生觀摩的一頁!
(基因體研究中心網頁資訊小組編製)
註一:
Xolair這個藥物的對象,是人體免疫系統自行生產的E型免疫球蛋白(IgE)。一般正常情況下,免疫球蛋白是為了防禦各類有害的病原體而生產,但由於現代化的生活環境,尤其都會區的人們長時間在密閉的空調環境中生活,因有些人的體質,會對一些原本無害的物質例如:花粉、塵蟎或寵物的皮屑等,稱為「過敏原(allergen)」的物質,產生過度敏感的免疫反應,IgE在體內逐漸累積。當累積超過某特定量,就誘發打噴嚏、流鼻水、氣管收縮之類的反應,這現象稱為「過敏(allergy)」。
Xolair是一人源化的(humanized)小鼠anti-IgE單株抗體,它結合IgE的位置,幾乎完全與IgE的高親和力受體(high-affinity receptor)結合IgE的位置相重疊,因此使IgE不能和IgE的高親和力受體結合。同理,Xolair也不會跨接(cross-linking)已結合在高親和力受體上的IgE。IgE與IgE的高親和力受體的結合在過敏反應的連串機制中有如子彈上膛,而跨接已結合在高親和力受體上的IgE則是有如扣下扳機。