為了在環境中生存,許多天然物配備了藥理活性,這也成為人們治療疾病聚焦的標的物。然而,天然物的生物活性機制多樣且複雜,在研發入藥的過程中,「副作用」的產生往往讓研究人員傷透了腦筋,如何去蕪存菁地將藥理活性發揮在醫療上,成為藥物開發前期的研究重點。
基因體研究中心鄭偉杰實驗室長期投入在生物鹼分子領域,本次研究發現是以苦馬豆素分子結構作為「核心骨架」,再以更換周邊取代基的方式,重新合成出約有四百多種變化的分子群,並將這些化合物進行篩選,最終找到了具有藥效且無副作用的新型小分子抑制劑。經由細胞與動物實驗的驗證,這個抑制劑不僅具有殺死肝癌細胞的效果,也降低了天然物作為藥物帶來的副作用。這項研究成果已經發表在英國皇家學院的旗艦期刊化學科學(Chemical Science)。
人體蛋白質表面的醣類影響了細胞的功能;將不同的醣聚合物支鏈連結到蛋白質表面的加工處理過程,是由酶來管控,因此常被當作是藥物標的。然而,同一個體系下,不同的酶,卻因為擁有相同的活化位點,讓不應當抑制的代謝功能一起受到干擾,造成體內機制的不平衡,進而出現副作用。
這個現象早在半世紀前就出現了,科學家在天然植物瘋馬草內,找到名為苦馬豆素的成分,是一種雙環亞胺醣生物鹼,它能抑制人體高爾基體α-甘露糖苷酶II (α-hGMII),達到改變癌細胞內蛋白質表面的的聚醣組態,進而限制腫瘤發展及轉移。但當進入臨床實驗時,卻發現它針對特定酵素的專一性不足,在抑制甘露糖苷酶II時,也會同時抑制細胞內的溶小體α-甘露糖苷酶(α-hLM),造成醣類在腦內堆積,導致溶小體儲積症的嚴重副作用,因而中止了苦馬豆素作為抗癌藥物的研發。
「藥物對於標的專一性不夠,就會連帶影響到其他功能,造成嚴重的副作用。」鄭偉杰老師說明,「我們的目標就是針對甘露糖苷酶,合成出更具有專一性的抑制劑,也就是新型小分子藥物。」
然而,化學全合成不但繁瑣,更是費時耗力。為了解決這個困難,鄭偉杰老師實驗室從「由天然物所啟發之組合式化學」(Natural Product-Inspired Combinatorial Chemistry)的概念出發,從零開始,先合成出苦馬豆素中具有生物活性的主要結構,接著用不同的分子組塊修飾主要結構,產生四個具有不同環大小以及不同相對位置的「骨架」結構,每個骨架藉由組合式化學可以產出約100種化合物,藉此快速地打造出含有約400個化合物的類天然物生物鹼分子庫(library)。
鄭老師實驗室研究人員同時也是本文第一作者陳韋安,把這些分子庫形容成「彈藥庫(molecular arsenal)」,只要有新的應用目標出現,就從儲備彈藥庫中找出適當的分子,經過一番修飾之後上場備選。「我們不只有分子庫,曾經輪番上陣的分子骨架已經能集結成一個骨架分子庫。」
這套核心技術是一場時間和技術的考驗,憑藉的除了鄭偉杰老師口中的「傻勁」,還有研究團隊過去在組合式化學和不對稱化學合成經驗的不斷累積。巧妙的運用組合式化學的優勢,以簡單的組合概念來製備大量可供篩選的分子庫。
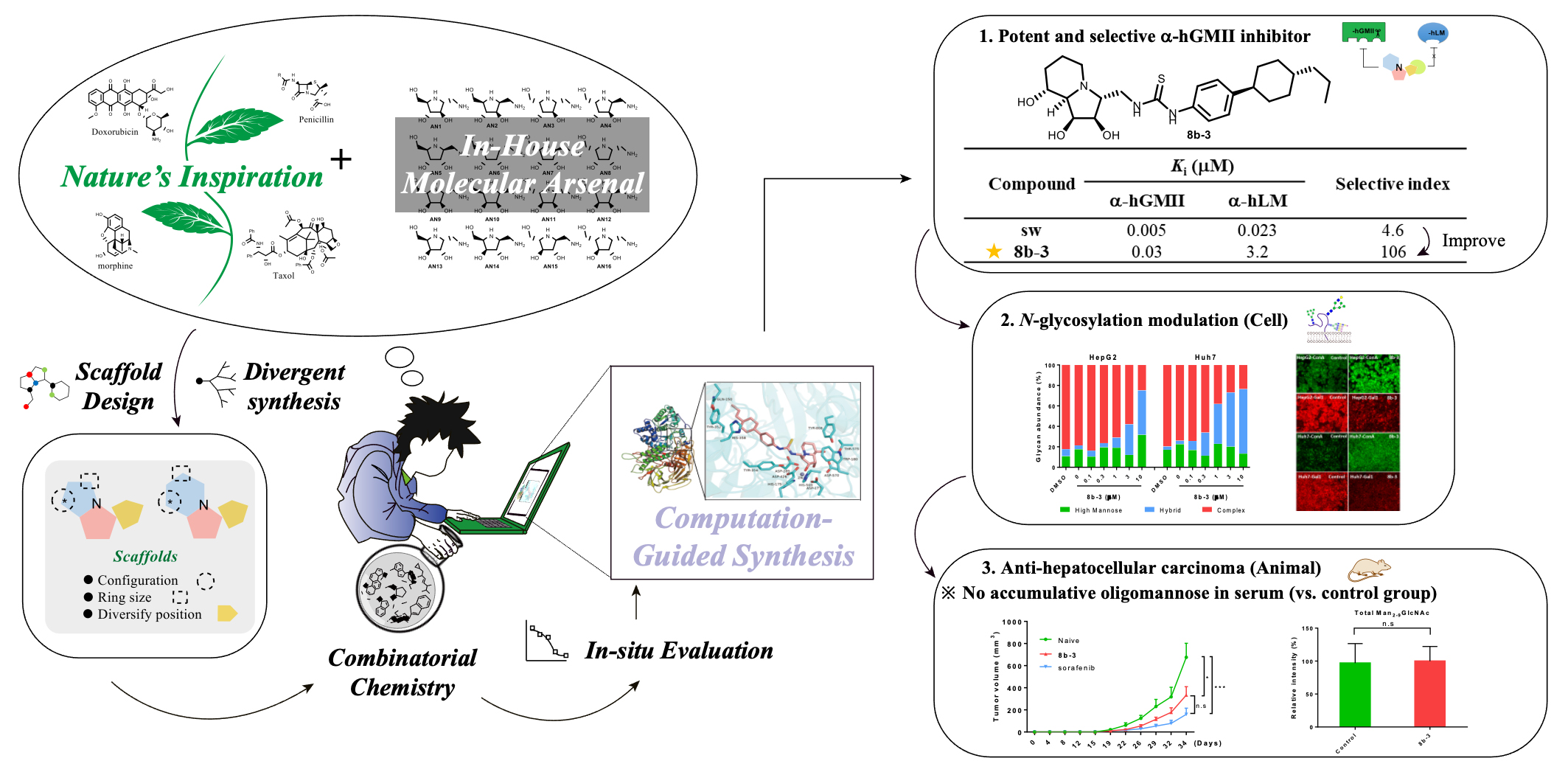 |
| 運用天然產物啟發的組合式化學合成技術平台,開發新型α-hGMII抑制劑。 |
在取得數目龐大、結構相似、但又有些細微差異的多樣性化合物之後,首要之務是篩選酵素活性。研究人員選定甘露糖苷酶II和α-甘露糖苷酶這兩種酵素進行篩選,找出對於甘露糖苷酶II專一性較高的分子,之後再利用電腦分子運算輔助預測,改良其功能及結構,優化分子結構,最後產出對於甘露糖苷酶II具有高度選擇性的有效小分子抑制劑ACK900。此新型分子抑制劑一舉將酵素選擇性指數從原天然物生物鹼的4倍提升到106倍。
研究團隊此次研發出來的小分子抑制劑ACK900,在細胞實驗中證實,相較於苦馬豆素,對於正常細胞具有較小的代謝物堆積副作用,並且能夠有效調節肝癌細胞的醣蛋白的聚醣組態,同時達到毒殺癌細胞以及抑制癌細胞轉移效果。
進一步的動物實驗也顯示,ACK900的抗癌效能和現有化療藥物索拉非尼(Sorafenib)相似。以ACK900作為藥物治療感染肝癌細胞的小鼠,追蹤後發現小鼠腫瘤縮小,顯示藥物能有效抑制肝癌生長。此外,血液生化數據也顯示此分子不具肝腎毒性,有效降低了細胞內溶小體聚醣堆積的副作用。
這項核心技術成功的讓因為嚴重副作用、止步於臨床研究長達30年的苦馬豆素展露曙光。此外,這低耗費、高產量的類天然物生物鹼分子庫,與傳統合成技術相比,創造出更具專一性的新型小分子,解決多年來無法以精確化學合成技術改變天然物分子結構的化學難題。
除了現正進行的肝癌實驗,團隊也在進行乳癌、胰臟癌和腦癌的測試。未來更是致力於將這首創從天然物中啟發的化學合成技術平台,廣泛地運用到藥物開發的探索,如與醣蛋白相關的自身免疫系統疾病。此外,也期望可運用於罕見疾病藥物及新一代抗生素的開發。
本研究集結多位基因體中心研究人員的專長,達成跨領域的合作,參與實驗室包含:鄭偉杰老師、沈家寧老師、鄭婷仁老師、吳盈達老師、林俊利老師、徐翠玲老師。研究成果已經申請美國臨時案專利,並發表在英國皇家學院的旗艦期刊化學科學(Chemical Science),同時榮獲評審團推薦為「2022化學科學熱門文章選集」(2022 Chemical Science HOT Article Collection)。
論文全文『Harnessing Natural-Product-Inspired Combinatorial Chemistry and Computation-Guided Synthesis to Develop N-Glycan Modulators as Anticancer Agents』。網址:https://pubs.rsc.org/en/content/articlelanding/2022/sc/d1sc05894k